الکترون نامتمرکز ( به انگلیسی: Delocalized electron ) به الکترون هایی در یک مولکول گفته می شود که متعلق به یک اتم یا پیوند خاص نیستند. این الکترون ها را می توان در سیستم های مزدوج و مزویونیک دید و نقش مهمی در نظریهٔ اوربیتال مولکولی دارند. الکترون های پیوند سیگما نیز نامتمرکزند.
در بنزن، ۶ اتم کربن، ۶ الکترون نامتمرکز که نتیجه پیوند پی هستند را در ساختار می دهند که با یک دایره در مرکز این مولکول نشان داده می شود. این که فاصلهٔ پیوندهای C - C در بنزن برابر است نیز نتیجهٔ این الکترون های نامتمرکز است.
در فلزها، هنگامی که الکترون های اوربیتال d با الکترون های اوربیتال s بالای خود تداخل داشته باشند، دریایی از الکترون های نامتمرکز در کل ساختار فلز درست می شود که توجیه گر پدیده هایی مانند رسانایی در فلزها هستند.
در گرافیت، هر اتم کربن می تواند ۳ تا از ۴ الکترون لایهٔ ظرفیت خود را در پیوند کووالانسی شرکت دهد و از این ۳ الکترون، یکی به صورت نامتمرکز خواهد بود که می تواند درون صفحه های گرافیت ( و نه عمود بر صفحه ها ) حرکت کند، از اینرو گرافیت در جهت برون صفحه رسانا و در جهت عمود بر صفحه هایش نارساناست. در الماس هر ۴ الکترون کربن متمرکزند و از این رو الماس نارساناست.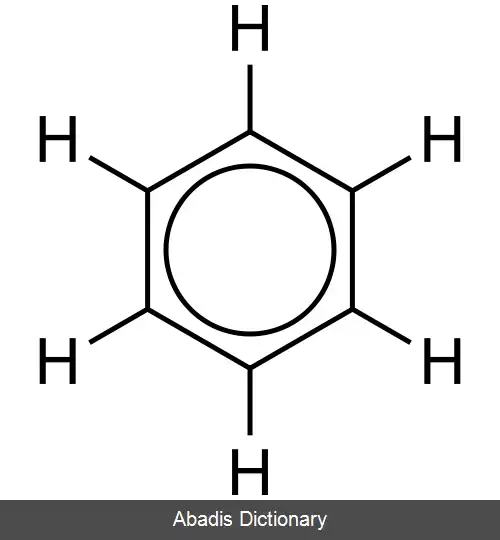
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفدر بنزن، ۶ اتم کربن، ۶ الکترون نامتمرکز که نتیجه پیوند پی هستند را در ساختار می دهند که با یک دایره در مرکز این مولکول نشان داده می شود. این که فاصلهٔ پیوندهای C - C در بنزن برابر است نیز نتیجهٔ این الکترون های نامتمرکز است.
در فلزها، هنگامی که الکترون های اوربیتال d با الکترون های اوربیتال s بالای خود تداخل داشته باشند، دریایی از الکترون های نامتمرکز در کل ساختار فلز درست می شود که توجیه گر پدیده هایی مانند رسانایی در فلزها هستند.
در گرافیت، هر اتم کربن می تواند ۳ تا از ۴ الکترون لایهٔ ظرفیت خود را در پیوند کووالانسی شرکت دهد و از این ۳ الکترون، یکی به صورت نامتمرکز خواهد بود که می تواند درون صفحه های گرافیت ( و نه عمود بر صفحه ها ) حرکت کند، از اینرو گرافیت در جهت برون صفحه رسانا و در جهت عمود بر صفحه هایش نارساناست. در الماس هر ۴ الکترون کربن متمرکزند و از این رو الماس نارساناست.

wiki: الکترون نامتمرکز
